





| 编号 | 1442 |
| 总例数 | 50例 |
| 性别例数 | 21例,女29例 |
| 治疗组例数 | 25例 |
| 对照组例数 | 25例 |
| 年龄区间 | 35~70岁 |
| 平均年龄 | 治疗组:平均(55.12±7.92)岁;对照组:平均(55.78±7.32)岁 |
| 疾病 | 2型糖尿病 |
| 并发症 | |
| 药品通用名称 | 那格列奈 |
| 药品商品名称 | |
| 药品英文名称 | Nateglinide |
| 剂型 | |
| 规格 | |
| 批准文号 | 国药准字H20030504 |
| 生产厂家 | 那格列奈:北京诺华制药有限公司生产 |
| 分类 | 化学药品 |
| 用药目的 | 治疗 |
| 用法用量 | 两组饮食、运动同前,在原治疗方案不变的基础上,A组加那格列奈(北京诺华制药有限公司生产,国药准字H20030504)治疗,开始剂量30mg,三餐前15分钟口服逐渐加量至120mg,三餐前15分钟口服;B组加格列齐特(贵州圣泉药业有限公司生产,国药准字H20003762)降糖治疗,开始剂量40mg,早晚餐前半小时口服逐渐加量至160mg,早、晚餐前半小时口服。 |
| 联合用药 | |
| 疗效评价标准 | |
| 治疗效果及临床指征比较 |
结果1. 降糖作用两组在治疗4周后FBG、2hPG均有显著下降(P<0.05),随着时间的延长,降糖作用更显著(P<0.01),对降低FBG,两组下降趋势是相同的,对于降低2hPG,那格列奈优于格列齐特;两组治疗前后HbA1C降低的幅度有统计学意义(P<0.05)。而InS两组均略有升高,但无统计学意义(P>0.05)。见表1。2. 对其它指标的影响在治疗12周后ALT、Cr、CHOL、TG与治疗前相比无统计学意义(P>0.05)。见表2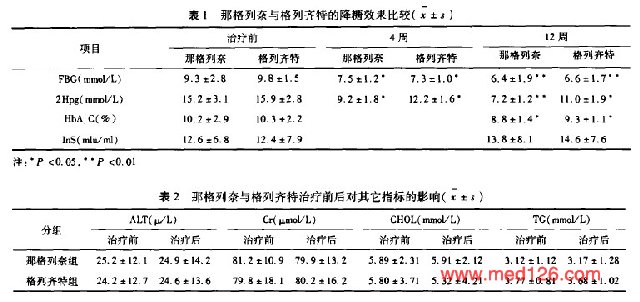 。 |
| 本研究报道不良反应 | 整个治疗过程中,A组患者未发现明显不良反应;B组有6例发生不良反应,其中低血糖反应4例,皮肤搔痒1例,腹泻1例。 |
| 其他报道不良反应 |